分泌型IgA是能确保宿主-微生物群落相互作用的关键粘膜组分,近日,一篇发表在国际杂志Nature Communications上题为“Dietary protein increases T-cell-independent sIgA production through changes in gut microbiota-derived extracellular vesicles”的研究报告中,来自悉尼大学等机构的科学家们通过进行一项临床前研究发现了一种高蛋白饮食或能改变肠道中的微生物群,从而诱发机体的免疫反应;本文研究结果或有望帮助更进一步理解饮食影响机体肠道健康和免疫力的方式。
研究人员的工作重点是揭示栖息在机体肠道中数以万亿的肠道菌群是如何影响免疫系统功能的,他们的最终目的就是理解如何操控这些肠道菌群来优化机体健康,而我们知道,改变微生物群落最简单的方法之一就是改变日常饮食,然而,从传统上来讲,科学家们一直专注于阐明膳食纤维在维持健康肠道中所扮演的关键角色。
这篇研究报告中,研究人员利用复杂的模型来深入揭示了10种含有不同洪亮营养素构成的饮食(包括蛋白质、脂质和碳水化合物等)对小鼠机体的影响,结果发现,高蛋白饮食或能改变肠道菌群的组成和活性,喂食高蛋白饮食的小鼠会增加细菌胞外囊泡的产生,这种胞外囊泡是一种含有诸如DNA和蛋白质等细菌信息的复杂“货物”,随后机体会将这种活动视为一种威胁,并诱发一系列事件,从而促使免疫细胞进入肠道壁中。
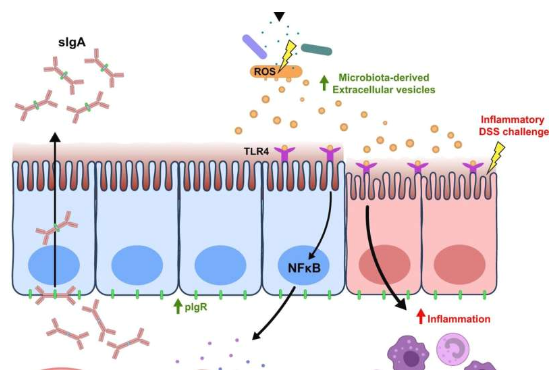
科学家揭开饮食、肠道健康和机体免疫力之间的神秘关联。
图片来源:Nature Communications (2022). DOI: 10.1038/s41467-022-31761-y
研究者Macia表示,在这里我们发现,蛋白质或会对机体肠道微生物群产生巨大的影响,而这与肠道中的细菌类型或许无关,而是与其活动的类型有关;从本质上来讲,我们发现了肠道菌群和宿主之间的一种新型沟通方式,其主要是通过蛋白质所介导的。尽管目前说这项研究可能能转化到人类机体中还为时尚早,但研究人员表示,免疫系统的激活或许就能证明是好消息或坏消息。通过增加肠道中抗体的产生,研究人员就能观察到机体抵御潜在病原体(比如沙门氏菌)的强大保护能力,但从负面来看,激活的免疫系统或许就意味着机体患结肠炎(一种炎性肠病)或诸如克罗恩病等自身免疫性疾病的风险会增加。
这一研究结果或许与现代人的饮食对机体的影响是一致的,西方世界人群的胃肠道感染率普遍较低,但其慢性疾病的发生率较高。Simpson教授表示,营养几何学(nutritional geometry)框架能促使我们根据食物的营养组分将食物、饮食和饮食模式绘制在一起,这或许能帮助研究人员观察到某些饮食、健康和疾病之间的关联中原本被忽略的一些模式。本文研究是研究人员首次将这种模型应用于免疫学研究。综上,本文研究中,研究人员建立了膳食宏量营养素组成、肠道菌群胞外囊泡释放以及宿主机体分泌型IgA反应之间的神秘关联。(生物谷Bioon.com)